Acétamipride
| Acétamipride | |
| |
| Identification | |
|---|---|
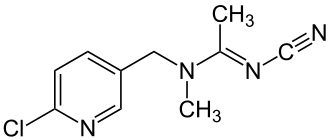
| Nom UICPA | (1E)-N-[(6-chloro-3-pyridyl)méthyl]-N'-cyano-N-méthylacétamidine |
| No CAS | (mélange de stéréoisomères Z et E) |
| No ECHA | 100.111.622 |
| PubChem | 213021 |
| ChEBI | 39164 |
| SMILES | |
| InChI | |
| Apparence | poudre blanche inodore[1] |
| Propriétés chimiques | |
| Formule | C10H11ClN4 [Isomères] |
| Masse molaire[2] | 222,674 ± 0,012 g/mol C 53,94 %, H 4,98 %, Cl 15,92 %, N 25,16 %, |
| pKa | 0,7 à 25 °C[1] |
| Propriétés physiques | |
| T° fusion | 98,9 °C[1] |
| Solubilité | 4,25 g·l-1 (eau, 25 °C)[1] |
| Précautions | |
| SGH[3] | |
 |
|
| Écotoxicologie | |
| LogP | 0,8 à 20 °C[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
L'acétamipride est un insecticide de la famille des néonicotinoïdes (NNi) mis au point à la fin des années 1990. Il est très utilisé, dans le monde entier, principalement dans la culture des végétaux.
En raison de son écotoxicité, il est interdit depuis 2018 en France dans ce domaine d'utilisation ; mais en 2025, malgré des études récentes montrant que sa toxicité sur les poissons, les mammifères et les abeilles semble avoir été antérieurement sous-estimée (parfois démontrée pour des expositions sub-léthales), une proposition de loi propose d'autoriser à nouveau son usage (ainsi que celui du flupyradifurone), à la demande de plusieurs filières, dont celle de la betterave sucrière et de la noisette.
Utilisations
L'acétamipride, produit industriellement depuis la fin des années 1990 comme pesticide systémique, est aujourd'hui surtout utilisé contre les insectes suceurs dans les cultures de végétaux feuillus, d'agrumes, de piridions (pommes, poires...), dans la vigne, dans la culture de coton et sur des espèces du genre Brassica (choux, colza, rutabaga, navet, moutarde, plantes ornementales...)[1], ainsi que des fruits à coques (noisette notamment). C'est également un pesticide clé dans la culture de la cerise en raison de son efficacité contre la larve de la mouche de la cerise, mais il a aussi d'autres usages dits non agricoles, autorisés ou non selon les pays :
- Lutte contre les insectes domestiques, par exemple sous forme de gel, en seringue ou sous forme de spray pour éliminer les cafards, les fourmis et autres espèces non désirées dans les habitations[4] ;
- Protection de plantes ornementales, dans les jardins, parcs et serres, contre les insectes suceurs.
- Traitement des bois et matériaux : Il peut être intégré dans certains produits pour protéger le bois contre les attaques d'insectes xylophages[réf. nécessaire].
Propriétés physicochimiques
L'acétamipride est un composé organochloré de formule brute C10H11ClN4. Il est inodore.
Comme d'autres néonicotinoïdes, ce produit est neurotoxique pour les insectes : il agit sur les récepteurs de l'acétylcholine de type nicotinique de leurs neurones[5].
Il existe un isomère de ce composé qui ne dépend que de la configuration de la double liaison.
Biodégradation
Ce produit est considéré comme relativement rapidement biodégradable. De nombreux microorganismes le dégradent mais peu d’études ont cherché à comprendre par quels mécanismes sous-jacents. Sun Shilei et ses collègues ont étudié ces mécanismes (enzymatiques notamment, qui impliquent les cytochromes P450, les hydratases nitrile, les amidases et les nitralases) et l'éventuelle toxicité de ses métabolites intermédiaires. Ces travaux doivent aussi contribuer à trouver des solutions de décontamination des milieux pollués par ce pesticide, par exemple à l'aide d'hydratases nitrile[6] par exemple trouvée dans la bactérie filamenteuse actinomycète Streptomyces canus CGMCC 13662 (isolé du sol) qui se montre capable de dégrader l'Acétamipride en IM-1-2 ((E)-1-(1-(((6-chloropyridin-3-yl)méthyl)(méthyl) amino)éthylidène)urée) par hydrolyse de l’entité cyanoïmine[7].
Écotoxicité et toxicité
L'acétamipride a un potentiel de bioaccumulation élevé[8]. Il est hautement toxique pour les oiseaux et vers de terre, et modérément toxique pour les organismes aquatiques[8]. L'utilisation excessive de ce pesticide constitue une menace pour les populations d'oiseaux et d'autres parties de la chaîne alimentaire.
Quand il est utilisé en pulvérisation foliaire, une part importante du produit (surfactant y compris) est emportée par le vent (phénomène de dérive) et/ou tombe au sol, où elle affecte notamment les arthropodes (l'essentiel de la biomasse animale du sol) ; Une étude récente (2024) faite en laboratoire avec des doses réalistes a confirmé une toxicité pour le collemboles (Folsomia candida) alors que les acariens du sol ont semblé peu sensible à ce pesticide ; cette différences de vulnérabilité peut perturber l'équilibre écologique des arthropodes du sol en bouleversant leur rapports d'abondance et de diversité ; en effet, l'étude a comparé des échantillons (issus de champs non traités) : avant l'exposition ; puis 7 et 54 jours plus tard, et ce, pour des concentrations croissantes d'acétamipride (0, 0,05, 0,2 et 0,8 mg par kg de sol sec)[9]. Cette comparaison a montré un déséquilibre, persistant plusieurs semaines après la dégradation du produit : forte diminution du nombre et de la variété des collemboles (-53 % à la dose la plus élevée), corrélativement à une hausse de la population d'acariens (+26 %). Il a fallu attendre près de 2 mois (54 jours) pour que la communauté semble se reconstituer, ce qui fait évoquer de possibles effets secondaires sur les services écosystémiques rendus par les sols[9].
« Il a été autorisé alors qu'on savait peu de choses des effets nocifs des néonicotinoïdes sur les vertébrés aquatiques » notaient en 2019 Ma Xue et al. Or, lessivé par les pluies, il peut atteindre les eaux superficielles et les zones humides où il est déjà dans les années 2020 « fréquemment détecté »[10]. En laboratoire, il s'avère toxique pour les embryons de poisson-zèbre (Danio rerio, une espèce-modèle communément utilisée par les écotoxicologues) : il faut atteindre 263 mg/litre pour observer « une mortalité significative et des effets tératogènes, la colonne vertébrale courbée étant la principale malformation (...) l’altération des mouvements spontanés était le paramètre le plus sensible de ceux testés »)[11], mais des effets subléthaux existent pour les larves. Or, à titre d'exemple, les résidus de ce pesticide, quantifiés dans quatre réservoirs d'eau du nord du Bénin au moment du traitement phytosanitaire du coton, varient de 0,2 à 7,7 μg L-1, des niveaux réputés non toxique pour l'Homme, mais qui signent un usage massif et régulier d’acétamipride (probablement associé à d’autres pesticides possiblement plus nocifs) et susceptible d'affecter les espèces aquatiques[12]. Les larves de Tilapia (l'une des espèces les plus couramment élevées et consommées en Afrique) s'y montrent également vulnérables[13] alors que celles du poisson-chat africain Clarias gariepinus, autre espèces très consommée s'y montrent pas ou moins sensibles[14].
Combiné au cadmium, qui est un polluant métallique agricole, néphrotoxique pour l'Homme, de plus en plus présent (contaminant des engrais), il inhibe la croissance des larves de poisson-zèbre et est source de malformations congénitales morphologiques[10]. Les analyse métabolomique montrent que ce pesticide, chez le poisson au stade larvaire, altère le métabolisme des riboflavines, le métabolisme des glycolipides et celui des acides aminés[10].
Les effets combinés de cette molécule avec ceux de divers adjuvants semblent aussi avoir été sous-estimés (ou non étudiés) ; une étude récente (2019) a testé ces effets pour trois adjuvants courants de pesticides, qui à eux seuls n'induisent pas de toxicité aiguë sur l'abeille, mais qui lors des tests de laboratoire accroissent significativement la toxicité de l'acetamipride pour l'abeille domestique[15].
Effets sur la biodiversité
Largement utilisé comme insecticide, l’acétamipride soulève des préoccupations environnementales en raison de ses effets directs et indirects sur les écosystèmes[16].
Il contribue à la réduction significative des populations d’arthropodes prédateurs tels que les acariens, mais aussi de pollinisateur et de parasitoïdes (parasites de parasites). Bien que certains acariens utiles puissent développer une résistance, leur comportement et leur efficacité en tant qu'agents de lutte biologique sont perturbés, ce qui favorise une augmentation des infestations de ravageurs[16].
Dans les régions où ce produit est encore utilisé, chez les oiseaux, des études révèlent une contamination généralisée, par exemple chez le merle, le martinet ou le colibri[16].
Dans les sols, bien que l’acétamipride soit moins persistant que d'autres néonicotinoïdes (DT50 inférieure à 2 jours), sa mobilité le rend susceptible de migrer vers les plantes ou les cours d’eau. Cette mobilité influence son impact écologique, puisqu'il figure parmi les trois néonicotinoïdes les plus fréquemment retrouvés dans les eaux douces. Une baisse de la diversité microbienne semble aussi augmenter la quantité d’acétamipride transférée du sol vers les plantes[16].
L’acétamipride affecte également les invertébrés du sol, notamment les vers de terre, qui présentent alors des troubles de la reproduction, une altération des tissus et une diminution de l’activité enzymatique liée à la décomposition des matières organiques[16].
Bien que l’acétamipride soit moins persistant que certains néonicotinoïdes, sa fréquence élevée de détection, sa toxicité pour divers organismes et ses effets indirects sur les chaînes alimentaires mettent ainsi en évidence son rôle dans la dégradation des écosystèmes[16].
Effets sur l'abeille domestique
Au début des années 2000, des études sur l'abeille domestique ont estimé que la DL50 de l'acétamipride est de 7,1 μg, avec un intervalle de confiance à 95 % de 4,57-11,2 μg/abeille[17].
Les métabolites produits après l'absorption de l'acétamipride par l'abeille domestique sont moins toxiques que ceux des autres néonicotinoïdes. La demi-vie de l'acétamipride est assez brève, environ 25 à 30 minutes, alors que d'autres néonicotinoïdes peuvent avoir une demi-vie de 4 à 5 heures. Cependant, certains métabolites sont toujours présents dans l'abeille domestique après 72 heures. Cela pourrait constituer un risque toxicologique pour ces abeilles, car une exposition chronique peut augmenter la toxicité de certains composés[18]. L'EPA le considère comme « modérément toxique » pour les abeilles ; malgré cela, certaines sources médiatiques et le documentaire Vanishing of the Bees ont accusé les néonicotinoïdes comme l'acétamipride de provoquer un syndrome d'effondrement des colonies.
Effets sub-léthaux
Selon une étude récente (2023), bien qu'individuellement peu toxique pour les abeilles domestiques aux doses environnementales normales (par rapport à d'autres pesticides), l'acétamipride, en laboratoire et à des concentrations imitant la contamination environnementale, n'affecte pas significativement le microbiote intestinal d'une espèce voisine (l'abeille asiatique ; Apis cerana) ; dans ces conditions, l'exposition prolongée au pesticide seul n'a pas significativement affecté la survie ni la consommation alimentaire des abeilles. Mais celles qui ont été exposées au difénoconazole ou au mélange acétamipride-difénoconazole ont présenté une « composition bactérienne intestinale altérée, contrairement aux colonies exposées uniquement à l'acétamipride »[19]. De plus, dans ce dernier cas, « les pesticides ont modifié l'expression des gènes liés à la détoxification, et la co-exposition à l'acétamipride et au difénoconazole a montré des effets toxiques plus prononcés à l'échelle moléculaire que l'exposition individuelle » ; les auteurs soulignent certaines limites de l'étude, et recommandent des expérimentations en conditions réelles« pour mieux comprendre les effets des pesticides sur le microbiome intestinal des abeilles et les mécanismes moléculaires impliqués »[19]. Il montre aussi des effets synergétiques significatifs quand il se combine ou est combiné avec d'autres substances. Environ 45 % des mélanges testés contenant de l'acétamipride et d'autres pesticides ont montré des interactions synergiques. Ces mélanges incluent notamment l'acétamipride combinée avec le tétraconazole, un fongicide. Ces effets synergétiques augmentent la toxicité globale, posant ainsi une menace accrue aux pollinisateurs en comparaison avec l'exposition à l'acétamipride seul. Même des doses sublétales d'acétamipride et du fongicide propiconazole, réalistes sur le terrain, peuvent provoquer des effets synergiques graves sur la survie, la santé et la physiologie des abeilles : augmentation significative de la mortalité, réduction du poids corporel, perturbation enzymatique, stress oxydatif accru[20].
Effets sur les larves des abeilles domestiques
Ces effets ont été confirmés, et précisés, par Jingliang et al en 2020[21], puis par d'autres études :
Même pour une exposition sublétale (0,5 et 25 mg/L), l'acétamipride perturbe le métabolisme des larves d'abeilles Apis mellifera[22], au moins en perturbant le métabolisme de l'hémolymphe des larves, avec en outre des effets sur le comportement et l'expression génique. Les profils métaboliques des abeilles exposées sont significativement modifiés ; 36 métabolites différents ont été identifiés, dont 19 régulés à la hausse et 17 à la baisse. Parmi 10 autres métabolites détectés, 3 étaient régulés à la hausse et 7 à la baisse. Parmi les composés affectés figurent l'acide traumatique et l'indole connus pour leur rôle essentiel et d'autres altérations des voies métaboliques, étaient liées à des perturbations du tryptophane, des purines et de la phénylalanine, qui suggèrent un impact direct de l'acétamipride sur la biochimie des larves. Selon les auteurs : « les dommages augmentent quand la concentration d'acétamipride dans l'alimentation (de la larve) dépasse 5 mg/L, entraînant des déséquilibres métaboliques notables »[22].
En 2024, Tadei et al. ont montré que l'acétamipride à faible dose (7 ng/L administrée via la nourriture aux abeilles femelles et mâles durant 48 h, suivies par 48 h supplémentaires sans nourriture contaminée, pour un total de 96 h d'observation) altère la locomotion (comportement léthargique) et la réponse phototactique de l'abeille solitaire Centris analis ; un effet qui disparait après 48 heures de retour à une alimentation non contaminée[23].
Bien que couramment utilisé sur les cultures pollinisées par les bourdons, ses effets sur les colonies de bourdon avait été peu étudiés, jusqu'à ce qu'une étude basée sur Bombus impatiens exposé, en microcolonies artificielles, à des pollens volontairement contaminés, montre — qu'à forte dose (4 520 μg d'Acétamipride par kg de pollen) — ce pesticides affecte négativement la croissance de la colonie, le développement des individus et la productivité, avec notamment une moindre production de mâles (effets qui disparaissent sous 45,2 μg/kg) Des études supplémentaires sont nécessaires pour évaluer l'impact de l'acétamipride via d'autres voies d'exposition que l'ingestion de pollen (et en présence des surfactants et autres additifs qui, fréquemment, exacerbent fortement la toxicité des pesticides)[24], et sur de vraies colonies sauvages.
L'analyse des bactéries intestinales d'abeilles domestiques exposées à l'acéamipride a montré qu'une partie de l'intestin de ces abeilles a été envahi par des bactéries opportunistes et pathogènes, ce qui a entrainé une chute de la richesse et la diversité des communautés du microbiote symbiotique de ces abeilles. Mais une supplémentation de la nourriture par un probiotique Apilactobacillus kunkeei (déjà aussi proposé comme probiotique pour l'Homme)[25] a considérablement augmenté (de 84 % à 92 %) le taux de survie des abeilles mellifères exposées à du pollen contaminé par de l'acétamipride, en permettant une certaine amélioration de la structure et de la stabilité du microbiote intestinal des abeilles supplémentées[26].
« Ces résultats soulignent l'importance de prendre en compte les effets sublétaux dans l'évaluation des risques environnementaux » concluaient en 2024 Rafaela Tadéi et ses collègues[23].
Toxicité humaine
Il a une faible toxicité aiguë et chronique chez les mammifères sans preuve de cancérogénicité, de neurotoxicité ou de mutagénicité. Il est classé dans la catégorie de toxicité II dans les études orales aiguës sur des rats, dans la catégorie de toxicité III dans les études cutanées aiguës et par inhalation sur des rats, et dans la catégorie de toxicité IV dans les études d'irritation oculaire et cutanée primaire sur des lapins. Il est mobile dans le sol, mais s'y dégrade rapidement par métabolisation aérobie, des études montrant une demi-vie comprise entre inférieure à 8,2 jours. L'EPA ne le considère pas comme persistant dans l'environnement.
D'après une étude de 2015, l'acétamipride serait une des causes de dysfonction érectile et, par là même, d'infertilité masculine[27].
Deux cas d'intoxication aiguë par ingestion d'un mélange insecticide contenant de l'acétamipride ont été décrits lors d'une tentative de suicide. Les deux patients ont été transportés aux urgences dans les deux heures qui ont suivi et ont immédiatement ressenti des nausées, une faiblesse musculaire, des convulsions et une température corporelle basse (33,7 °C et 34,3 °C respectivement). Les symptômes tels que la faiblesse musculaire semblent être similaires à ceux de l'exposition à un insecticide organophosphoré. L'hypothermie et les convulsions peuvent être directement expliquées par le composé actif d'acétamipride qui réagit avec les récepteurs nicotiniques et de l'acétylcholine. Bien que la toxicité de ce pesticide pour les mammifères soit considérée comme faible, des doses élevées d'acétamipride sont considérées comme toxiques pour les humains[28].
Effets sur le système nerveux central et l'anxiété
En 2022, Hirai et ses collègues, au Japon, alertent sur le fait que les néonicotinoïdes en général sont associés à une augmentation de certains dysfonctionnements neurologiques chez les mammifères ; avec notamment un effet anxiogène restés longtemps incompris (mais confirmé au Japon, sur la souris de laboratoire, même à une dose réputée sans effet nocif observé (NOAEL), de 20 mg/kg (dose fixée par la Commission de sécurité alimentaire du Japon)[29].
Cet effet a été attribué aux monoamines (MA)[29], « des neurotransmetteurs impliqués dans le contrôle du comportement, de la mémoire et de l’apprentissage ». A cette dose, les souris soumises à un test de labyrinthe après administration du pesticide montrent un stress anxieux, mesuré par leurs niveaux de dopamine, 3-MT, sérotonine et histamine. Et leurs taux de neurotransmetteurs est modifié dans plusieurs régions du cerveau, avec des changements de taux de sérotonine hippocampique, de dopamine striatale qui sont corrélés à l'anxiété[30]. L'immunomarquage a confirmé une activation des neurones sérotoninergiques dans les noyaux du raphé, une zone connue comme étant impliquée dans l'anxiété. Dans le modèle murin, l'acétamipride, en affectant la sérotonine hippocampique, active bien une anxiété, concluent les auteurs[30] (un phénomène qui avait déjà été observé, également à la dose dose NOAEL, pour un autre pesticide de cette même famille des néonicotinoïdes : la clothianidine, repéré dans ce cas par des cris de stress émis par les souris mâles exposées à de faibles doses de cette molécule)[31].
Marques et fabricants
L'acétamipride est vendu sous les marques Assail, Pristine, Chipco par Aventis CropSciences et Supreme par Certis Europe[32].
Acétamipride et potabilisation de l'eau
Miyashiro et Hamoudi (2022) ont proposé un système non chimique de dégradation aqueuse de l’acétamipride, combinant l'ultrasonication et une photocatalyse sous lumière visible[33].
Phénomènes de résistance
On observe en Afrique la diffusion préoccupante de moustiques (vecteurs du paludisme, notamment) à la fois résistants aux pyréthrinoïdes et aux néonicotinoïdes, par exemple dans les fermes maraîchères du nord du Bénin[34].
Interdiction en France
Dans le domaine agricole, cette molécule est interdite en France dans les produits phytopharmaceutiques depuis le [35]. Par dérogation, l'interdiction a été repoussée à 2020 pour la protection contre le balanin des noisettes, les mouches du figuier et les pucerons du navet[36]. Il reste autorisé partout ailleurs en Europe. Les 5[37] néonicotinoïdes interdits sont ainsi l’acétamipride, le clothianidine, l’imidaclopride, le thiaclopride et le thiaméthoxame.
En 2025, une proposition de loi portée par le sénateur Laurent Duplomb contient la réintroduction dérogatoire de l’acétamipride. Cette disposition est réclamée par les producteurs de betteraves sucrières et de noisettes, avançant n'avoir aucune autre solution pour protéger efficacement leurs cultures. La FNSEA et la Coordination rurale, dénoncent une « concurrence déloyale » avec les autres producteurs européens et une « porte ouverte aux importations », notamment de noisettes produites avec des pesticides interdits en France. Le texte suscite de vifs débats[38].
Références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « acetamiprid » (voir la liste des auteurs).
- 1 2 3 4 5 6 fiche de l'EPA (Environmental Protection Agency - United States)
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Erreur de référence : Balise
<ref>incorrecte : aucun texte n’a été fourni pour les références nomméesGESTIS - ↑ GREGORY, « Quel gel anti-cafard choisir ? », sur Blattes & Cafards, (consulté le )
- ↑ Bodereau-Dubois, B. (2011). Récepteurs nicotiniques neuronaux d'insectes et insecticides: caractérisation de facteurs cellulaires impliqués dans la modulation de l'efficacité des néonicotinoïdes (Doctoral dissertation, Angers) (résumé).
- ↑ (en) Shilei Sun, Jiangsheng Zhou, Jihong Jiang et Yijun Dai, « Nitrile Hydratases: From Industrial Application to Acetamiprid and Thiacloprid Degradation », Journal of Agricultural and Food Chemistry, vol. 69, no 36, , p. 10440–10449 (ISSN 0021-8561 et 1520-5118, DOI 10.1021/acs.jafc.1c03496, lire en ligne, consulté le )
- ↑ (en) Ling Guo, Wen-Wan Fang, Lei-Lei Guo et Chuan-Fei Yao, « Biodegradation of the Neonicotinoid Insecticide Acetamiprid by Actinomycetes Streptomyces canus CGMCC 13662 and Characterization of the Novel Nitrile Hydratase Involved », Journal of Agricultural and Food Chemistry, vol. 67, no 21, , p. 5922–5931 (ISSN 0021-8561 et 1520-5118, DOI 10.1021/acs.jafc.8b06513, lire en ligne, consulté le )
- 1 2 (en)University of Hertfordshire, 2018. Pesticide Properties DataBase. "acetamiprid". (Archive)
- 1 2 (en) Michella Ligtelijn, S. Henrik Barmentlo et Cornelis A.M. van Gestel, « Field-realistic doses of the neonicotinoid acetamiprid impact natural soil arthropod community diversity and structure », Environmental Pollution, vol. 359, , p. 124568 (DOI 10.1016/j.envpol.2024.124568, lire en ligne, consulté le )
- 1 2 3 (en) Guixian Hu, Hao Wang, Jiahong Zhu et Liangliang Zhou, « Combined toxicity of acetamiprid and cadmium to larval zebrafish (Danio rerio) based on metabolomic analysis », Science of The Total Environment, vol. 867, , p. 161539 (DOI 10.1016/j.scitotenv.2023.161539, lire en ligne, consulté le )
- ↑ (en) Xue Ma, Huizhen Li, Jingjing Xiong et W. Tyler Mehler, « Developmental Toxicity of a Neonicotinoid Insecticide, Acetamiprid to Zebrafish Embryos », Journal of Agricultural and Food Chemistry, vol. 67, no 9, , p. 2429–2436 (ISSN 0021-8561 et 1520-5118, DOI 10.1021/acs.jafc.8b05373, lire en ligne, consulté le )
- ↑ (en) Berny’s G. Y. M. Zoumenou, Martin P. Aïna, Ibrahim Imorou Toko et Ahmed Igout, « Occurrence of Acetamiprid Residues in Water Reservoirs in the Cotton Basin of Northern Benin », Bulletin of Environmental Contamination and Toxicology, vol. 102, no 1, , p. 7–12 (ISSN 0007-4861 et 1432-0800, DOI 10.1007/s00128-018-2476-4, lire en ligne, consulté le )
- ↑ (en) Nicresse L. Guedegba, Ibrahim Imorou Toko, Prudencio T. Agbohessi et Berny’s Zoumenou, « Comparative acute toxicity of two phytosanitary molecules, lambda-cyhalothrin and acetamiprid, on Nile Tilapia ( Oreochromis Niloticus ) juveniles », Journal of Environmental Science and Health, Part B, vol. 54, no 7, , p. 580–589 (ISSN 0360-1234 et 1532-4109, DOI 10.1080/03601234.2019.1616986, lire en ligne, consulté le )
- ↑ (en) Mahugnon A. B. Houndji, Ibrahim Imorou Toko, Léa Guedegba et Edith Yacouto, « Joint toxicity of two phytosanitary molecules, lambda-cyhalothrin and acetamiprid, on African catfish ( Clarias gariepinus ) juveniles », Journal of Environmental Science and Health, Part B, vol. 55, no 7, , p. 669–676 (ISSN 0360-1234 et 1532-4109, DOI 10.1080/03601234.2020.1763712, lire en ligne, consulté le )
- ↑ (en) Lang Chen, Qingping Yan, Jinzhen Zhang et Shankui Yuan, « Joint Toxicity of Acetamiprid and Co-Applied Pesticide Adjuvants on Honeybees under Semifield and Laboratory Conditions », Environmental Toxicology and Chemistry, vol. 38, no 9, , p. 1940–1946 (ISSN 0730-7268 et 1552-8618, DOI 10.1002/etc.4515, lire en ligne, consulté le )
- 1 2 3 4 5 6 Laure Mamy, Stéphane Pesce, Wilfried Sanchez, Marcel Amichot, Joan Artigas, et al.. Impacts des produits phytopharmaceutiques sur la biodiversité et les services écosystémiques. Rapport de l’expertise scientifique collective. [Rapport de recherche] INRAE; IFREMER. 2022, 1408 p. ⟨hal-03777257⟩ DOI 10.17180/0gp2-cd65
- ↑ Motohiro Tomizawa, John E. Casida, (2003). Selective Toxicity of Neonicotinoids Attributable to Specificity of Insect and Mammalian Nicotinic Receptors". Annual Review of Entomology. 48 (1): 339–364. DOI 10.1146/annurev.ento.48.091801.112731
- ↑ Brunet, J.-L., Badiou, A. and Belzunces, L.P. (2005), In vivo metabolic fate of [14C]-acetamiprid in six biological compartments of the honeybee, Apis mellifera L. Pest. Manag. Sci., 61: 742-748. DOI 10.1002/ps.1046
- 1 2 Wensu Han, Zheyuan Ye, Yifan Gu et Yihai Zhong, « Gut microbiota composition and gene expression changes induced in the Apis cerana exposed to acetamiprid and difenoconazole at environmentally realistic concentrations alone or combined », Frontiers in Physiology, vol. 14, (ISSN 1664-042X, PMID 37256066, PMCID 10226273, DOI 10.3389/fphys.2023.1174236, lire en ligne, consulté le )
- ↑ Han, W., Yang, Y., Gao, J. et al., Chronic toxicity and biochemical response of Apis cerana cerana (Hymenoptera: Apidae) exposed to acetamiprid and propiconazole alone or combined. Ecotoxicology 28, 399–411 (2019). DOI 10.1007/s10646-019-02030-4
- ↑ (en) Jingliang Shi, Ruonan Zhang, Yalin Pei et Chunhua Liao, « Exposure to acetamiprid influences the development and survival ability of worker bees (Apis mellifera L.) from larvae to adults », Environmental Pollution, vol. 266, , p. 115345 (DOI 10.1016/j.envpol.2020.115345, lire en ligne, consulté le )
- 1 2 (en) Xinxin Shi, Jingliang Shi, Longtao Yu et Xiaobo Wu, « Metabolic profiling of Apis mellifera larvae treated with sublethal acetamiprid doses », Ecotoxicology and Environmental Safety, vol. 254, , p. 114716 (DOI 10.1016/j.ecoenv.2023.114716, lire en ligne, consulté le )
- 1 2 Rafaela Tadei, Claudia Inês da Silva, Elaine C. Mathias da Silva et Osmar Malaspina, « Effects of the insecticide acetamiprid and the fungicide azoxystrobin on locomotion activity and mushroom bodies of solitary bee Centris analis », Chemosphere, vol. 364, , p. 143254 (ISSN 0045-6535, DOI 10.1016/j.chemosphere.2024.143254, lire en ligne, consulté le )
- ↑ (en) Christopher A. Mullin, Jing Chen, Julia D. Fine et Maryann T. Frazier, « The formulation makes the honey bee poison », Pesticide Biochemistry and Physiology, vol. 120, , p. 27–35 (DOI 10.1016/j.pestbp.2014.12.026, lire en ligne, consulté le )
- ↑ (en) Franca Vergalito, Bruno Testa, Autilia Cozzolino et Francesco Letizia, « Potential Application of Apilactobacillus kunkeei for Human Use: Evaluation of Probiotic and Functional Properties », Foods, vol. 9, no 11, , p. 1535 (ISSN 2304-8158, PMID 33113800, PMCID 7693146, DOI 10.3390/foods9111535, lire en ligne, consulté le )
- ↑ (en) Peng Liu, Jingheng Niu, Yejia Zhu et Zhuang Li, « Apilactobacillus kunkeei Alleviated Toxicity of Acetamiprid in Honeybee », Insects, vol. 13, no 12, , p. 1167 (ISSN 2075-4450, PMID 36555077, PMCID 9784809, DOI 10.3390/insects13121167, lire en ligne, consulté le )
- ↑ « Potential pathways of pesticide action on erectile function – A contributory factor in male infertility », Asian Pacific Journal of Reproduction, vol. 4, no 4, , p. 322–330 (ISSN 2305-0500, DOI 10.1016/j.apjr.2015.07.012, lire en ligne, consulté le )
- ↑ Tomonori Imamura, Youichi Yanagawa, Kahoko Nishikawa, Naoto Matsumoto & Toshihisa Sakamoto (2010). Two cases of acute poisoning with acetamiprid in humans, Clinical Toxicology, 48:8, 851-853. DOI 10.3109/15563650.2010.517207
- 1 2 (en) Anri Hirai, Ryo Yamazaki, Atsushi Kobayashi et Takashi Kimura, « Detection of Changes in Monoamine Neurotransmitters by the Neonicotinoid Pesticide Imidacloprid Using Mass Spectrometry », Toxics, vol. 10, no 11, , p. 696 (ISSN 2305-6304, DOI 10.3390/toxics10110696, lire en ligne, consulté le )
- 1 2 (en) Anri Hirai, Chitoku Toda, Yared Beyene Yohannes et Nimako Collins, « Role of brain monoamines in acetamiprid-induced anxiety-like behavior », Toxicology, vol. 505, , p. 153839 (DOI 10.1016/j.tox.2024.153839, lire en ligne, consulté le )
- ↑ (en) Tetsushi Hirano, Shogo Yanai, Tadashi Takada et Naoki Yoneda, « NOAEL-dose of a neonicotinoid pesticide, clothianidin, acutely induce anxiety-related behavior with human-audible vocalizations in male mice in a novel environment », Toxicology Letters, vol. 282, , p. 57–63 (DOI 10.1016/j.toxlet.2017.10.010, lire en ligne, consulté le )
- ↑ MAP/e-PHY, « Spécialité : SUPREME », sur e-phy.agriculture.gouv.fr (consulté le ).
- ↑ (en) Carolina Sayury Miyashiro et Safia Hamoudi, « Aqueous Acetamiprid Degradation Using Combined Ultrasonication and Photocatalysis Under Visible Light », Water, Air, & Soil Pollution, vol. 233, no 10, (ISSN 0049-6979 et 1573-2932, PMID 36168646, PMCID 9508044, DOI 10.1007/s11270-022-05867-4, lire en ligne, consulté le )
- ↑ (en) Massioudou Koto Yérima Gounou Boukari, Innocent Djègbè, Ghislain T. Tepa-Yotto et Donald Hessou-Djossou, « Cross-Resistance to Pyrethroids and Neonicotinoids in Malaria Vectors from Vegetable Farms in the Northern Benin », Tropical Medicine and Infectious Disease, vol. 9, no 12, , p. 305 (ISSN 2414-6366, DOI 10.3390/tropicalmed9120305, lire en ligne, consulté le )
- ↑ LOI no 2016-1087 du 8 août 2016 pour la reconquête de la biodiversité, de la nature et des paysages, article 125
- ↑ Légifrance, du 7 mai 2019 portant dérogation à l'interdiction d'utilisation de produits phytopharmaceutiques contenant une ou des substances actives de la famille des néonicotinoïdes et des semences traitées avec ces produits mentionnée à l'article L. 253-8 du code rural et de la pêche maritime
- ↑ Décret no 2018-675 du 30 juillet 2018 relatif à la définition des substances actives de la famille des néonicotinoïdes présentes dans les produits phytopharmaceutiques.
- ↑ Qu’est-ce que l’acétamipride, ce pesticide décrié dans la proposition de loi «Duplomb» ?, lefigaro.fr, 26 mai 2025
Voir aussi
Articles connexes
Bibliographie
- (en) Asma Verdian, « Apta-nanosensors for detection and quantitative determination of acetamiprid – A pesticide residue in food and environment », Talanta, vol. 176, , p. 456–464 (DOI 10.1016/j.talanta.2017.08.070, lire en ligne, consulté le ).
- Portail de la chimie
- Portail de l’agriculture et l’agronomie
- Portail de la protection des cultures
- Portail de l’entomologie