Hormones prénatales et orientation sexuelle
La théorie hormonale de la sexualité soutient que, tout comme l’exposition à certaines hormones joue un rôle dans la différenciation sexuelle du fœtus, cette exposition influence également l’orientation sexuelle qui émerge plus tard chez l’individu. Les hormones prénatales peuvent être considérées comme le principal déterminant de l’orientation sexuelle à l’âge adulte, ou comme un cofacteur.
Comportement typé selon le sexe
La théorie hormonale de la sexualité soutient que, tout comme l’exposition à certaines hormones joue un rôle dans la différenciation sexuelle du fœtus, cette exposition influence également l’orientation sexuelle qui émerge plus tard à l’âge adulte. On pense que les différences dans la structure du cerveau qui résultent de l’interaction des messagers chimiques et des gènes sur les cellules cérébrales en développement sont à la base des différences entre les sexes dans d’innombrables comportements, y compris l’orientation sexuelle[1]:25. Les facteurs prénataux qui affectent ou interfèrent avec l’interaction de ces hormones sur le cerveau en développement peuvent influencer le comportement sexuel ultérieur des enfants[1]:24. Cette hypothèse est issue d’études expérimentales sur des mammifères non humains, mais l’argument selon lequel des effets similaires peuvent être observés dans le développement neurocomportemental humain est un sujet très débattu parmi les chercheurs[2]. Des études récentes ont cependant fourni des preuves à l’appui de l’hypothèse selon laquelle l’exposition prénatale aux androgènes influencerait le comportement sexué de l’enfant[2].
Les hormones fœtales peuvent être considérées soit comme l’influence principale sur l’orientation sexuelle adulte, soit comme un cofacteur interagissant avec les gènes[3]. Garcia-Falgueras et Dick Swaab ne sont pas d’accord sur le fait que les conditions sociales influencent dans une large mesure l’orientation sexuelle. Comme on le constate chez les jeunes enfants ainsi que chez les vervets bleus ou les macaques rhésus, le comportement différencié selon le sexe dans la préférence pour les jouets diffère chez les mâles et les femelles, où les femelles préfèrent les poupées et les mâles préfèrent les balles et les voitures jouets ; ces préférences peuvent être observées dès 3 à 8 mois chez les humains[2]. Il est impossible d’exclure complètement l’environnement social ou la compréhension cognitive du genre par l’enfant lorsqu’on discute du jeu typé selon le sexe chez les filles exposées aux androgènes[2]. À l’inverse, les enfants ont tendance à préférer les objets qui ont été étiquetés pour leur propre sexe, ou les jouets avec lesquels ils ont déjà vu des membres de leur sexe jouer[2].
Une étude d'endocrinologie menée par Garcia-Falgueras et Swaab a postulé que « chez l'homme, le principal mécanisme responsable de [sic] l'identité et l'orientation sexuelles implique un effet direct de la testostérone sur le développement du cerveau. »[1]:25En outre, leur étude suggère que l’exposition intra-utérine aux hormones est largement déterminante. En simplifiant leur argumentation, les auteurs affirment que les organes sexuels se différencient en premier, puis le cerveau se différencie sexuellement « sous l'influence, principalement, des hormones sexuelles telles que la testostérone, l'œstrogène et la progestérone sur les cellules cérébrales en développement et sous la présence de différents gènes également... Les changements apportés à ce stade sont permanents... La différenciation sexuelle du cerveau n'est pas causée uniquement par les hormones, même si elles sont très importantes pour l'identité de genre et l'orientation sexuelle. »[1]:24
Aspects organisationnels
Les gonades embryonnaires se développent principalement en fonction de la présence ou non d'un gène SRY, normalement présent sur le chromosome Y. Si le SRY existe, alors les gonades se développent en testicules et commencent la production d'hormones androgènes, principalement la testostérone, la dihydrotestostérone (DHT) et l'androstènedione ; la production de testostérone et la conversion en dihydrotestostérone au cours des semaines 6 à 12 de la grossesse sont des facteurs clés dans la production du pénis, du scrotum et de la prostate d'un fœtus mâle[4]. Chez la femme, en revanche, l’absence de ces niveaux d’androgènes entraîne le développement d’organes génitaux typiquement féminins[4]. À la suite de cela, la différenciation sexuelle du cerveau se produit ; les hormones sexuelles exercent des effets organisationnels sur le cerveau qui seront activés à la puberté[4]. En raison de la séparation de ces deux processus, le degré de masculinisation génitale n’est pas nécessairement lié à la masculinisation du cerveau[1]:24,[4] Des différences entre les sexes ont été constatées dans de nombreuses structures cérébrales, notamment dans l’ hypothalamus et l’ amygdale[2]. Cependant, peu d’entre eux ont été liés à des différences comportementales entre les sexes, et les scientifiques travaillent toujours à établir des liens solides entre les hormones précoces, le développement du cerveau et le comportement[2]. L'étude de la théorie organisationnelle des hormones prénatales peut se révéler complexe car, d'un point de vue éthique, les chercheurs ne peuvent pas modifier les hormones d'un fœtus en développement ; au lieu de cela, les chercheurs doivent s'appuyer sur des anomalies naturelles du développement pour fournir des réponses[5].
L'hyperplasie congénitale des surrénales (HCS) est l'une des maladies les plus étudiées en ce qui concerne les effets organisationnels des hormones[6]. L’HCA est une maladie génétique qui entraîne une exposition à des niveaux élevés d’androgènes dès le début de la gestation. Les filles atteintes d'HCS naissent avec des organes génitaux masculinisés, qui sont corrigés chirurgicalement dès que possible[5],[6]. La CAH offre la possibilité de réaliser des expériences naturelles, car les personnes atteintes de CAH peuvent être comparées à celles qui n’en sont pas atteintes. Cependant, « l'HCS n'est pas une expérience parfaite », car « les réponses sociales aux organes génitaux masculinisés ou les facteurs liés à la maladie elle-même » peuvent brouiller les résultats[5]. Néanmoins, plusieurs études ont montré que l'HCS a une influence claire mais non déterminante sur l'orientation sexuelle ; les femmes atteintes d'HCS sont moins susceptibles d'être exclusivement hétérosexuelles que les autres femmes[6].
Étant donné que les hormones seules ne déterminent pas l'orientation sexuelle et la différenciation du cerveau, la recherche d'autres facteurs agissant sur l'orientation sexuelle a conduit à impliquer des gènes tels que SRY et ZFY[7].
Stress maternel prénatal
En 2006, les résultats d'études sur les humains ont révélé des preuves contradictoires concernant l'effet de l'exposition prénatale aux hormones et les résultats psychosexuels ; Gooren a noté en 2006 que les études sur les mammifères non-primates ne permettent pas de réaliser des mesures valides de la différenciation sexuelle humaine, car les hormones sexuelles suivent un rôle plus « on-off » dans le comportement sexuel que celui que l'on trouve chez les primates[8].
Certaines études suggèrent que le stress prénatal augmente considérablement la probabilité d’homosexualité ou de bisexualité, bien que les preuves varient quant au trimestre le plus important[1]:24. Des études en endocrinologie ont également montré que les amphétamines et les hormones thyroïdiennes augmentaient l'homosexualité chez les filles, bien que cela n'ait pas été examiné en conjonction avec les niveaux de stress prénatal[1]:24.
Certains ont postulé que le développement postnatal (par exemple, les facteurs sociaux et environnementaux) peut jouer un rôle dans l’orientation sexuelle d’un individu, mais aucune preuve solide de cette hypothèse n’a été apportée jusqu'ici. Les enfants nés par insémination artificielle avec sperme de donneur et par conséquent élevés par des couples de lesbiennes ont généralement une orientation hétérosexuelle[1]:24[4]. Comme le résument Bao et Swaab, « l'apparente impossibilité de faire changer d'orientation sexuelle quelqu'un... est un argument majeur contre l'importance de l'environnement social dans l'émergence de l'homosexualité, ainsi que contre l'idée que l'homosexualité est un choix de vie. »[4]
Ordre de naissance fraternel
Selon une multitude d’études menées sur plusieurs décennies, les hommes homosexuels ont en moyenne davantage de frères aînés, un phénomène connu sous le nom d’effet d’ordre de naissance fraternel. Il a été suggéré que plus le nombre de frères et sœurs aînés est élevé, plus le niveau d’androgènes auquel les fœtus sont exposés est élevé. Aucune preuve d’effets liés à l’ordre de naissance n’a été observée chez les femmes. La théorie soutient que l'effet de l'ordre de naissance fraternel est le résultat d'une réponse immunitaire maternelle qui se produit contre un facteur de développement masculin au cours de plusieurs grossesses masculines[9]. L'hypothèse d'Anthony Bogaert est que « la cible de la réponse immunitaire pourrait être des molécules spécifiques aux mâles à la surface des cellules cérébrales fœtales mâles (par exemple, y compris celles de l'hypothalamus antérieur). Les anticorps anti-mâles pourraient se lier à ces molécules et ainsi interférer avec leur rôle dans la différenciation sexuelle normale, conduisant certains mâles nés plus tard à être attirés par les hommes plutôt que par les femmes. »[9] Garcia-Falgueras et Swaab affirment que « l'effet de l'ordre de naissance fraternel... s'explique par une réponse immunologique de la mère à un produit du chromosome Y de ses fils. La probabilité d'une telle réponse immunitaire aux facteurs masculins augmenterait à chaque grossesse aboutissant à la naissance d'un fils. »[1]:24
Des anticorps maternels contre la neuroligine du chromosome Y ont été impliqués dans cet effet[10], parmi d'autres preuves qui appuient cette théorie[11]. De plus, bien que l’on estime que la probabilité d’homosexualité augmente de 15[11] à 48 % par frère aîné, ces probabilités ne concernent en réalité que quelques pour cent de la population ; par conséquent, cette hypothèse ne peut pas être appliquée universellement à la majorité des hommes homosexuels[8]. La plupart des études[12], mais pas toutes, ont pu reproduire l’effet de l’ordre de naissance fraternel. Certains n'ont pas trouvé de différence statistiquement significative dans la composition de la fratrie ou dans le taux de frères aînés des hommes homosexuels et hétérosexuels[13],[14], y compris de grandes études représentatives à l'échelle nationale aux États-Unis et au Danemark[15],[16]. Cependant, Blanchard a réanalysé l'étude danoise de Frisch de 2006 et a découvert que l'effet de l'ordre de naissance était effectivement présent[17].
En conjonction avec l’ordre de naissance fraternel, la latéralité fournit une preuve supplémentaire des effets prénataux sur l’orientation sexuelle, car la latéralité est considérée par beaucoup comme un marqueur du développement neurologique précoce. D'autres corrélats de la latéralité (par exemple, la latéralité cérébrale, les profils hormonaux prénataux, l'habileté de construction visuo-spatiale) ont été liés à l'orientation sexuelle, de manière empirique et/ou théorique[9]. Chez les individus droitiers, le nombre de frères aînés augmentait les risques d’orientation homosexuelle, mais cet effet n’était pas observé chez les individus gauchers[9]. Cependant, comme pour d’autres signes présumés indiquant une incidence plus élevée d’homosexualité, le lien avec la latéralité reste ambigu et plusieurs études n’ont pas été en mesure de le reproduire[18],[19],[20].
Gènes impliqués dans l'ordre de naissance fraternel
Un gène du système Rh a été évoqué comme candidat potentiel pour affecter l'ordre de naissance fraternel, car il a été lié à la fois à la latéralité et au fonctionnement du système immunitaire[9]. Les variantes génétiques du système Rh sont impliquées dans une réponse maternelle à ce que l’on appelle la maladie hémolytique du nouveau-né . Le Rh est un facteur présent dans le sang et dans les cas où la mère en est dépourvue ( Rh- ) alors qu'elle porte un fœtus Rh+, une réponse immunitaire peut se développer avec des effets délétères. L'hypothèse du gène Rh est un candidat sérieux car il est impliqué dans la réponse immunitaire maternelle, mais également la latéralité[9].
Des variantes du gène du récepteur des androgènes (AR) ont également été étudiées, dans la mesure où le fait d'être non droitier chez les hommes a été associé à un plus grand nombre de répétitions CAG dans le gène AR, qui à son tour est associé à un taux de testostérone plus faible. Une théorie selon laquelle un taux élevé de testostérone prénatale entraîne une perte neuronale et axonale dans le corps calleux est appuyée par cette hypothèse[21].
Il existe des preuves que les mutations dans NLGN4X et NLGN4Y sont liées aux troubles du spectre autistique[22],[23] et que ces troubles peuvent être plus fréquents chez les personnes asexuées[24]. Ainsi, NLGN4X/Y peut affecter le fonctionnement neurologique associé, de manière générale, à la formation de liens sociaux avec les autres, y compris les liens sexuels/romantiques.
Théorie thyroïdienne prénatale de l'homosexualité/dysphorie de genre
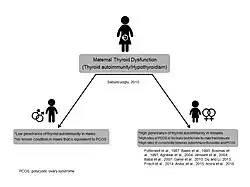
La théorie thyroïdienne prénatale de l'attirance pour les personnes de même sexe/dysphorie de genre est basée sur des observations cliniques et développementales de jeunes se présentant dans des cliniques de psychiatrie infantile à Istanbul. Le rapport de 12 cas d'attirance pour le même sexe/dysphorie de genre nés de mères atteintes de maladies thyroïdiennes a été présenté pour la première fois au congrès de l'EPA, à Vienne (2015) et publié sous forme d'article la même année[25],[26]. La relation extrêmement significative entre les deux conditions a suggéré un modèle indépendant, appelé modèle thyroïdien prénatal de l'homosexualité. Selon le psychiatre turc pour enfants et adolescents Osman Sabuncuoglu, à l'origine de cette théorie, un dysfonctionnement de la thyroïde maternelle peut entraîner des déviations anormales du développement spécifique au sexe de la progéniture. Le processus de destruction auto-immune observé dans la thyroïdite de Hashimoto, la diminution de l'apport d'hormones thyroïdiennes et les impacts sur le système androgène prénatal ont tous été considérés comme des mécanismes contributifs. Dans un article théorique de suivi[27], des résultats de recherche antérieurs indiquant des taux plus élevés de syndrome des ovaires polykystiques (SOPK) chez les transsexuels femme-homme et les femmes lesbiennes ont été conçus comme une indication du modèle thyroïdien prénatal puisque le SOPK et la thyroïdite auto-immune sont fréquemment des maladies comorbides. De même, les taux accrus de troubles du spectre autistique chez les enfants nés de mères souffrant de dysfonctionnement thyroïdien et la surreprésentation des personnes atteintes de TSA dans les populations atteintes de dysphorie de genre suggèrent une telle association. Un deuxième groupe de jeunes enfants présentant ce modèle a été présenté au congrès IACAPAP, à Prague (2018)[28]. De plus, 9 cas supplémentaires ont été signalés lors du congrès de l'IACAPAP, à Rio de Janeiro (Sabuncuoglu, 2024).
Les résultats de recherches antérieures sur les populations LGBT ont conduit les chercheurs à s'intéresser au système thyroïdien[29],[30]. Un commentaire de Jeffrey Mullen, publié peu de temps après l’article de 2015, a souligné l’importance du modèle thyroïdien prénatal et a soutenu les développements dans ce domaine[31]. Par la suite, plusieurs auteurs ont souligné le rôle du système thyroïdien dans la sexualité en citant le modèle thyroïdien prénatal.[32],[33],[34],[35] Parmi eux, Carosa et al. ont conclu que les hormones thyroïdiennes, affectant fortement la fonction sexuelle humaine, la glande thyroïde doit être considérée, avec les organes génitaux et le cerveau, comme un organe sexuel[32]. En tant que source tertiaire, un livre faisant autorité sur le sujet de l'interaction entre l'endocrinologie, le cerveau et le comportement a également cité l'article sur la proposition thyroïde-homosexualité dans la dernière édition. Plus important encore, une étude d’association génétique à l’échelle du génome sur les homosexuels masculins a identifié une région importante sur le chromosome 14 qui est liée au dysfonctionnement thyroïdien auto-immun chez les êtres humains[36]. Il s’agit apparemment d’un soutien important au modèle thyroïdien prénatal.
Homosexualité masculine et hypermasculinité
Il existe des preuves d’une corrélation entre l’orientation sexuelle et les traits déterminés in utero[3]. Une étude réalisée par McFadden en 1998 a révélé que les systèmes auditifs du cerveau, un autre trait physique influencé par les hormones prénatales, sont différents chez les personnes d'orientations différentes ; de même, Swaab et Hofman ont découvert que le noyau suprachiasmatique (SCN) était plus grand chez les hommes homosexuels que chez les hommes hétérosexuels[37]. On sait également que le noyau suprachiasmatique est plus gros chez les hommes que chez les femmes[38]. Une analyse de l'hypothalamus par Swaab et Hofman (1990;2007) a révélé que le volume du SCN chez les hommes homosexuels était 1,7 fois plus grand que celui d'un groupe de référence de sujets masculins et contenait 2,1 fois plus de cellules[8],[39]. Au cours du développement, le volume du SCN et le nombre de cellules atteignent leur valeur maximale environ 13 à 16 mois après la naissance ; à cet âge, le SCN contient le même nombre de cellules que celui trouvé chez les homosexuels mâles adultes, mais dans un groupe de référence d'hommes hétérosexuels, le nombre de cellules commence à diminuer jusqu'à la valeur adulte de 35 % de la valeur maximale[8]. Ces résultats ont été reproduits et ont confirmé les conclusions. Cependant, il reste encore à fournir une interprétation significative de ces résultats dans le contexte de l’orientation sexuelle humaine[8]. Certaines études très controversées suggèrent que les hommes homosexuels auraient également des niveaux plus élevés d'androgènes circulants[40],[41],[42] et des pénis plus grands[43], en moyenne, que les hommes hétérosexuels.
Homosexualité masculine comme hypomasculinité
Dans une étude de 1991, Simon LeVay a démontré qu'un minuscule groupe de neurones de l'hypothalamus antérieur — qui est censé contrôler le comportement sexuel et être lié aux hormones prénatales — connu sous le nom de noyaux interstitiels de l'hypothalamus antérieur était, en moyenne, plus de deux fois plus grand chez les hommes hétérosexuels que chez les hommes homosexuels. Étant donné que cette zone est presque deux fois plus grande chez les hommes hétérosexuels que chez les femmes hétérosexuelles, on peut en déduire que la différenciation sexuelle de l'hypothalamus chez les homosexuels se fait dans le sens féminin[8]. En 2003, des scientifiques de l'Université d'État de l'Oregon ont annoncé qu’ils avaient reproduit ses découvertes sur des moutons.
D'autres preuves ont montré l'inverse : il a été démontré que le SCN des hommes homosexuels est plus grand (le volume et le nombre de neurones sont deux fois plus nombreux que chez les hommes hétérosexuels), ce qui contredit l'hypothèse selon laquelle les hommes homosexuels ont un « hypothalamus féminin »[44]. William Byne et ses collègues ont également pesé et compté le nombre de neurones dans les tests INAH 3 non-réalisés par LeVay. Les résultats pour le poids de l'INAH3 étaient similaires à ceux pour la taille de l'INAH3 ; c'est-à-dire que le poids de l'INAH3 pour les cerveaux des hommes hétérosexuels était significativement plus grand que pour les cerveaux des femmes hétérosexuelles, tandis que les résultats pour le groupe des hommes homosexuels se situaient entre ceux des deux autres groupes, mais pas tout à fait significativement différents de l'un ou l'autre[45]. Enfin, la même recherche a révélé que le volume de l' INAH3 est plus petit chez les hommes homosexuels que chez les hommes hétérosexuels, car les hommes homosexuels ont une densité neuronale plus élevée dans l'INAH3 que les hommes hétérosexuels ; il n'y a pas de différence dans le nombre ou la surface transversale des neurones dans l'INAH3 des hommes homosexuels par rapport aux hommes hétérosexuels[46].
Homosexualité féminine
La plupart des recherches empiriques ou théoriques sur l’orientation sexuelle des femmes ont, historiquement, été guidées par l’idée selon laquelle les lesbiennes sont essentiellement masculines et les femmes hétérosexuelles essentiellement féminines[47]. En général, cette croyance remonte à la première « théorie de l'inversion » des chercheurs en sexualité qui affirment que l'homosexualité est le résultat d'anomalies biologiques qui « inversent » l'attirance sexuelle et la personnalité[47]. Les recherches sur la latéralité ont fourni des implications ; étant donné que davantage d’hommes que de femmes présentent une préférence pour leur main gauche, la proportion plus élevée de non-droitiers qui a été découverte chez les lesbiennes par rapport aux femmes hétérosexuelles démontre un lien possible entre la masculinisation prénatale et l’orientation sexuelle[47]. Les rapports qui étayent ces conclusions sont basés sur des données recueillies auprès d'au moins six laboratoires différents, selon lesquelles les lesbiennes présentent des ratios d'indices de Manning plus masculinisés que les femmes hétérosexuelles[48]. Cet effet n’a pas encore été observé entre les hommes homosexuels et hétérosexuels[48]. Cependant, la validité de cette mesure du rapport des chiffres reste controversée en tant que prédicteur de l'androgène prénatal, car de nombreux autres facteurs prénatals peuvent jouer un rôle dans la croissance osseuse aux stades prénataux du développement[8]. Bien que de nombreuses études aient trouvé des résultats confirmant cette hypothèse, d’autres n’ont pas réussi à reproduire ces résultats[8], laissant la validité de cette mesure non confirmée.
Le diéthylstilbestrol (DES), un médicament qui a été prescrit dans le passé pour prévenir les fausses couches, a également été étudié en relation avec l’orientation sexuelle des femmes. Il a été observé qu'il exerce un effet masculinisant/déféminisant sur le développement du cerveau du fœtus[47]. Comparativement aux témoins, des pourcentages plus élevés de femmes exposées au DES (17 % contre 0 %) ont déclaré avoir eu des relations homosexuelles ; cependant, la grande majorité des femmes exposées au DES ont déclaré une orientation exclusivement hétérosexuelle[47].
Les filles atteintes d'hyperplasie congénitale des surrénales (une maladie autosomique récessive qui entraîne des niveaux élevés d'androgènes pendant le développement fœtal) ont des identités sexuelles plus masculinisées et sont plus susceptibles d'avoir une orientation sexuelle homosexuelle à l'âge adulte que les témoins[49],[50],[51],[52],[53]. Une explication alternative à cet effet est le fait que les filles atteintes de cette maladie naissent avec des organes génitaux externes masculinisés, ce qui conduit leurs parents à les élever de manière plus masculine, influençant ainsi leur orientation sexuelle à l’âge adulte. Cependant, le degré de masculinisation des organes génitaux des filles n’est pas corrélé à leur orientation sexuelle, ce qui suggère que les hormones prénatales sont un facteur causal plus fort, et non l’influence parentale.
Avec l'hyperplasie congénitale des surrénales, les études sur le DES ont fourni un soutien limité à la théorie de l'orientation sexuelle liée aux hormones prénatales ; elles fournissent cependant le cadre des voies possibles vers une orientation homosexuelle pour un petit nombre de femmes[47].
Dysphorie de genre
Chez les personnes atteintes de dysphorie de genre, anciennement connue sous le nom de trouble de l’identité de genre (TIG), on a émis l’hypothèse que l’exposition prénatale à la testostérone aurait un effet sur la différenciation de l’identité de genre. Le rapport 2D;4D des doigts (indice de Manning), ou les longueurs relatives du 2e (index) et du 4e (annulaire), est devenu une mesure populaire de l'androgène prénatal en raison des preuves accumulées suggérant que les rapports 2D;4D sont liés à l'exposition prénatale à la testostérone[54]. De nombreux enfants atteints de dysphorie de genre différencient une orientation homosexuelle pendant l'adolescence, mais pas tous ; les adultes ayant un « début précoce » ou des antécédents d'enfance de comportement intergenre ont souvent une orientation homosexuelle. Les adultes ayant un « début tardif », ou ceux qui n’ont pas d’antécédents d’enfance de ce comportement, sont plus susceptibles d’avoir une orientation non homosexuelle[54].
L'exposition prénatale aux androgènes a été associée à un risque accru de changement de sexe à l'initiative du patient après avoir été initialement élevé comme une femme dans la petite enfance ou la petite enfance[8],[55]. Gooren a constaté que les effets organisationnels des androgènes prénatals sont plus répandus dans le comportement de genre que dans l'identité de genre, et que des résultats préliminaires suggèrent que l'identité de genre masculine est plus fréquente chez les patients présentant une androgénisation prénatale entièrement typiquement masculine[8].
Les personnes atteintes du syndrome d’insensibilité complète aux androgènes sont presque toujours élevées comme des femmes, et la différenciation de l’identité/du rôle de genre est féminine[8]. Cet exemple est important pour démontrer que les chromosomes et les gonades seuls ne dictent pas l’identité et le rôle du genre[8].
Transsexualisme
Étant donné que la différenciation des organes et la différenciation du cerveau se produisent à des moments différents, dans de rares cas, le transsexualisme peut en résulter[1]:24.
S'appuyant sur certains cas de transsexualisme, Garcia-Falgueras et Swaab affirment que « ces exemples montrent que l'action directe de la testostérone sur le développement du cerveau chez les garçons et l'absence d'action sur le développement du cerveau chez les filles sont des facteurs cruciaux dans le développement de l'identité sexuelle et de l'orientation sexuelle masculine et féminine »[1]:26. D'innombrables études ont été menées sur les niveaux périphériques de stéroïdes sexuels chez les homosexuels hommes et femmes, dont un nombre considérable prétendaient trouver « moins d'hormones mâles et/ou plus d'hormones femelles chez les homosexuels hommes et vice versa chez les homosexuelles femmes »[8]. Cependant, ces résultats ont été examinés et ont ensuite été rejetés par Gooren comme souffrant d'une conception et d'une interprétation défectueuses[8].
Les facteurs impliqués dans le développement de la transsexualité comprennent les anomalies chromosomiques, les polymorphismes de certains gènes et les variations de l'aromatase (cytochrome P450 CYP19) et du CYP17[8]. Les filles atteintes d'hyperplasie congénitale des surrénales présentent une probabilité accrue de transsexualité plus tard dans la vie ; cependant, cette probabilité n'est encore que de 1 à 3 % dans le cas de l'HCA[8]. Bien que la différenciation sexuelle historiquement anormale ait pointé du doigt les androgènes comme facteur causal, il existe des codéterminants de l'identité de genre et de l'orientation sexuelle[8]. Ces facteurs sont actuellement inconnus et il n’existe donc pas de réponse claire à la cause du transsexualisme et de l’homosexualité[8].
De plus, en raison de la taille relativement petite des populations, les études sur la transsexualité sont peu généralisables.
Les perturbateurs endocriniens
Les perturbateurs endocriniens (PE) sont des substances chimiques qui, à certaines doses, peuvent interférer avec le système endocrinien des mammifères. Les travaux sur les éventuels effets neurotoxiques des perturbateurs endocriniens et leurs effets possibles sur l'orientation sexuelle lorsqu'un fœtus y est exposé en sont à leurs débuts : « nous connaissons principalement la relation entre l'exposition aux perturbateurs endocriniens et la fonction neurocomportementale grâce à un examen des résultats obtenus dans un spectre de questions limité. »[56] Bien que des études aient montré que les xénoestrogènes et les xénoandrogènes peuvent altérer la différenciation sexuelle du cerveau chez un certain nombre d'espèces utilisées comme modèles animaux[57], d'après les données disponibles à ce jour, il est « trompeur... de s'attendre à ce que les perturbateurs endocriniens produisent des profils d'effets, tels que des comportements sexuellement dimorphiques, comme des copies littérales de ceux produits par les hormones natives. De tels agents ne sont pas des hormones. On ne devrait pas s'attendre à ce qu'ils agissent exactement comme des hormones. »[56]
Références
- 1 2 3 4 5 6 7 8 9 10 11 Pediatric Neuroendocrinology, vol. 17, coll. « Endocrine Development », , 22–35 p. (ISBN 978-3-8055-9302-1, PMID 19955753, DOI 10.1159/000262525), « Sexual hormones and the brain: an essential alliance for sexual identity and sexual orientation ».
- 1 2 3 4 5 6 7 « Sex-related variation in human behavior and the brain », Trends in Cognitive Sciences, vol. 14, no 10, , p. 448–456 (PMID 20724210, PMCID 2951011, DOI 10.1016/j.tics.2010.07.005).
- 1 2 Wilson, G., & Q. Rahman, Born Gay: The Psychobiology of Human Sex Orientation, Peter Owen Publishers; 2d edition (May 1, 2008) (ISBN 9780720613094).
- 1 2 3 4 5 6 « Sexual differentiation of the human brain: relation to gender identity, sexual orientation and neuropsychiatric disorders », Frontiers in Neuroendocrinology, vol. 32, no 2, , p. 214–226 (PMID 21334362, DOI 10.1016/j.yfrne.2011.02.007, S2CID 8735185).
- 1 2 3 « Sexual differentiation of human behavior: effects of prenatal and pubertal organizational hormones », Frontiers in Neuroendocrinology, vol. 32, no 2, , p. 183–200 (PMID 21397624, DOI 10.1016/j.yfrne.2011.03.001, S2CID 205776417).
- 1 2 3 « Prenatal endocrine influences on sexual orientation and on sexually differentiated childhood behavior », Frontiers in Neuroendocrinology, vol. 32, no 2, , p. 170–182 (PMID 21333673, PMCID 3296090, DOI 10.1016/j.yfrne.2011.02.006).
- ↑ « The genetics of sex differences in brain and behavior », Frontiers in Neuroendocrinology, vol. 32, no 2, , p. 227–246 (PMID 20951723, PMCID 3030621, DOI 10.1016/j.yfrne.2010.10.001).
- 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 « The biology of human psychosexual differentiation », Hormones and Behavior, vol. 50, no 4, , p. 589–601 (PMID 16870186, DOI 10.1016/j.yhbeh.2006.06.011, S2CID 21060826).
- 1 2 3 4 5 6 « Interaction of birth order, handedness, and sexual orientation in the Kinsey interview data », Behavioral Neuroscience, vol. 121, no 5, , p. 845–853 (PMID 17907817, DOI 10.1037/0735-7044.121.5.845).
- ↑ « Sex differences in neuroimmunity as an inherent risk factor », Neuropsychopharmacology, vol. 44, no 1, , p. 38–44 (PMID 29977075, PMCID 6235925, DOI 10.1038/s41386-018-0138-1).
- 1 2 « Birth order, sibling sex ratio, handedness, and sexual orientation of male and female participants in a BBC internet research project », Archives of Sexual Behavior, vol. 36, no 2, , p. 163–176 (PMID 17345165, DOI 10.1007/s10508-006-9159-7, S2CID 18868548).
- ↑ « Fraternal Birth Order, Family Size, and Male Homosexuality: Meta-Analysis of Studies Spanning 25 Years », Archives of Sexual Behavior, vol. 47, no 1, , p. 1–15 (PMID 28608293, DOI 10.1007/s10508-017-1007-4, S2CID 10517373).
- ↑ « Do shared etiological factors contribute to the relationship between sexual orientation and depression? », Psychological Medicine, vol. 42, no 3, , p. 521–532 (PMID 21867592, PMCID 3594769, DOI 10.1017/S0033291711001577).
- ↑ « Fraternal Birth Order and Extreme Right-Handedness as Predictors of Sexual Orientation and Gender Nonconformity in Men », Archives of Sexual Behavior, vol. 44, no 5, , p. 1493–1501 (PMID 25663238, DOI 10.1007/s10508-014-0474-0, S2CID 30678785).
- ↑ « Family and sexual orientation: the family-demographic correlates of homosexuality in men and women », Journal of Sex Research, vol. 45, no 4, , p. 371–377 (PMID 18937128, DOI 10.1080/00224490802398357, S2CID 20471773).
- ↑ « Childhood family correlates of heterosexual and homosexual marriages: a national cohort study of two million Danes », Archives of Sexual Behavior, vol. 35, no 5, , p. 533–547 (PMID 17039403, DOI 10.1007/s10508-006-9062-2, S2CID 21908113).
- ↑ (en) « Reply to Blanchard's (2007) "Older-Sibling and Younger-Sibling Sex Ratios in Frisch and Hviid's (2006) National Cohort Study of Two Million Danes" », Archives of Sexual Behavior, vol. 36, no 6, , p. 864–867 (ISSN 1573-2800, DOI 10.1007/s10508-007-9169-0, S2CID 143749001).
- ↑ « Dermatoglyphics, handedness, sex, and sexual orientation », Archives of Sexual Behavior, vol. 31, no 1, , p. 113–122 (PMID 11910784, DOI 10.1023/A:1014039403752, S2CID 29217315).
- ↑ « Finger-length ratios and sexual orientation », Nature, vol. 404, no 6777, , p. 455–456 (PMID 10761903, DOI 10.1038/35006555, Bibcode 2000Natur.404..455W, S2CID 205005405).
- ↑ « Hair whorl direction and sexual orientation in human males », Behavioral Neuroscience, vol. 123, no 2, , p. 252–256 (PMID 19331448, DOI 10.1037/a0014816, S2CID 46164333).
- ↑ « Left out axons make men right: a hypothesis for the origin of handedness and functional asymmetry », Neuropsychologia, vol. 29, no 4, , p. 327–333 (PMID 1857504, DOI 10.1016/0028-3932(91)90046-B, S2CID 23754055).
- ↑ « Mutations of the X-linked genes encoding neuroligins NLGN3 and NLGN4 are associated with autism », Nature Genetics, vol. 34, no 1, , p. 27–29 (PMID 12669065, PMCID 1925054, DOI 10.1038/ng1136, S2CID 4798621).
- ↑ « Behavioral phenotypes in males with XYY and possible role of increased NLGN4Y expression in autism features », Genes, Brain and Behavior, vol. 14, no 2, , p. 137–144 (PMID 25558953, PMCID 4756915, DOI 10.1111/gbb.12200, S2CID 36755210).
- ↑ « Are Autism Spectrum Disorder and Asexuality Connected? features », Archives of Sexual Behavior, vol. 51, no 4, , p. 2091–2115 (PMID 34779982, DOI 10.1007/s10508-021-02177-4, S2CID 244115396).
- ↑ « Maternal Thyroid Dysfunction During Pregnancy May Lead to Same-sex Attraction/gender Nonconformity in the Offspring: Proposal of Prenatal Thyroid Model », European Psychiatry, vol. 30, , p. 374 (ISSN 0924-9338, DOI 10.1016/s0924-9338(15)30294-7, S2CID 143359069).
- ↑ « High Rates of Same-Sex Attraction/Gender Nonconformity in the Offspring of Mothers with Thyroid Dysfunction During Pregnancy: Proposal of Prenatal Thyroid Model », Mental Illness, vol. 7, no 2, , p. 5810 (PMID 26605033, PMCID 4620281, DOI 10.4081/mi.2015.5810).
- ↑ « Towards a further understanding of prenatal thyroid theory of homosexuality: Autoimmune thyroiditis, polycystic ovary syndrome, autism and low birth weight », Mental Illness, vol. 9, no 2, , p. 7325 (PMID 29142667, PMCID 5661141, DOI 10.4081/mi.2017.7325).
- ↑ « A second group of youngsters with gender nonconformity/same-sex attraction born to mothers with thyroid dysfunction in pregnancy », .
- ↑ Ellis et Hellberg, « Fetal exposure to prescription drugs and adult sexual orientation », Personality and Individual Differences, vol. 38, no 1, , p. 225–236 (ISSN 0191-8869, DOI 10.1016/j.paid.2004.04.004, lire en ligne).
- ↑ Frisch, Nielsen et Pedersen, « Same-sex marriage, autoimmune thyroid gland dysfunction and other autoimmune diseases in Denmark 1989-2008 », European Journal of Epidemiology, vol. 29, no 1, , p. 63–71 (ISSN 1573-7284, PMID 24306355, DOI 10.1007/s10654-013-9869-9, S2CID 11819672, lire en ligne).
- ↑ Mullen, « A link between maternal thyroid hormone and sexual orientation? », Mental Illness, vol. 8, no 1, , p. 6591 (ISSN 2036-7465, PMID 27403279, PMCID 4926038, DOI 10.4081/mi.2016.6591, lire en ligne).
- 1 2 Carosa, Lenzi et Jannini, « Thyroid hormone receptors and ligands, tissue distribution and sexual behavior », Molecular and Cellular Endocrinology, vol. 467, , p. 49–59 (ISSN 0303-7207, PMID 29175529, DOI 10.1016/j.mce.2017.11.006, hdl 11573/1132156, S2CID 36883213, lire en ligne).
- ↑ Basavanhally, Fonseca et Uversky, « Born This Way: Using Intrinsic Disorder to Map the Connections between SLITRKs, TSHR, and Male Sexual Orientation », Proteomics, vol. 18, nos 21–22, , p. 1800307 (ISSN 1615-9853, PMID 30156382, DOI 10.1002/pmic.201800307, S2CID 52115603, lire en ligne).
- ↑ Wang, Wu et Sun, « The biological basis of sexual orientation: How hormonal, genetic, and environmental factors influence to whom we are sexually attracted », Frontiers in Neuroendocrinology, vol. 55, , p. 100798 (ISSN 0091-3022, PMID 31593707, DOI 10.1016/j.yfrne.2019.100798, S2CID 203667616, lire en ligne).
- ↑ Roberto Castello et Marco Caputo, « Thyroid diseases and gender », Italian Journal of Gender-Specific Medicine, vol. 5, no 2019September–December, , p. 136–141 (DOI 10.1723/3245.32148, lire en ligne).
- ↑ Sanders, Beecham, Guo et Dawood, « Genome-Wide Association Study of Male Sexual Orientation », Scientific Reports, vol. 7, no 1, , p. 16950 (ISSN 2045-2322, PMID 29217827, PMCID 5721098, DOI 10.1038/s41598-017-15736-4, Bibcode 2017NatSR...716950S, lire en ligne).
- ↑ « Structural sex differences in the brain: influence of gonadal steroids and behavioral correlates », Journal of Endocrinological Investigation, vol. 18, no 3, , p. 232–252 (PMID 7615911, DOI 10.1007/BF03347808, S2CID 10435075).
- ↑ « Development of vasoactive intestinal polypeptide neurons in the human suprachiasmatic nucleus in relation to birth and sex », Brain Research. Developmental Brain Research, vol. 79, no 2, , p. 249–259 (PMID 7955323, DOI 10.1016/0165-3806(94)90129-5).
- ↑ « An enlarged suprachiasmatic nucleus in homosexual men », Brain Research, vol. 537, nos 1–2, , p. 141–148 (PMID 2085769, DOI 10.1016/0006-8993(90)90350-K, S2CID 13403716, lire en ligne).
- ↑ « Plasma testosterone levels in heterosexual and homosexual men », The American Journal of Psychiatry, vol. 131, no 1, , p. 82–83 (PMID 4808435, DOI 10.1176/ajp.131.1.82).
- ↑ « Further studies on sex hormones in male homosexuals », Archives of General Psychiatry, vol. 33, no 5, , p. 611–614 (PMID 1267577, DOI 10.1001/archpsyc.1976.01770050063010).
- ↑ « Sex differences in cognition: the role of testosterone and sexual orientation », Brain and Cognition, vol. 41, no 3, , p. 245–262 (PMID 10585237, DOI 10.1006/brcg.1999.1125, S2CID 44831103).
- ↑ « The relation between sexual orientation and penile size », Archives of Sexual Behavior, vol. 28, no 3, , p. 213–221 (PMID 10410197, DOI 10.1023/A:1018780108597, S2CID 42801275).
- ↑ « Gender and sexual orientation in relation to hypothalamic structures », Hormone Research, vol. 38 Suppl 2, no 2, , p. 51–61 (PMID 1292983, DOI 10.1159/000182597, hdl 20.500.11755/7cb8b769-4329-407a-b0ee-13e011017f68, lire en ligne).
- ↑ « The interstitial nuclei of the human anterior hypothalamus: an investigation of variation with sex, sexual orientation, and HIV status », Hormones and Behavior, vol. 40, no 2, , p. 86–92 (PMID 11534967, DOI 10.1006/hbeh.2001.1680, S2CID 3175414, lire en ligne).
- ↑ « The interstitial nuclei of the human anterior hypothalamus: an investigation of variation with sex, sexual orientation, and HIV status », Hormones and Behavior, vol. 40, no 2, , p. 86–92 (PMID 11534967, DOI 10.1006/hbeh.2001.1680, S2CID 3175414).
- 1 2 3 4 5 6 « Masculinity, Femininity and the Development of Sexual Orientation in Women », Journal of Gay & Lesbian Mental Health, vol. 12, nos 1–2, , p. 145–165 (DOI 10.1300/J529v12n01_09, S2CID 142691272).
- 1 2 « Genetic and environmental influences on 2D:4D finger length ratios: a study of monozygotic and dizygotic male and female twins », Archives of Sexual Behavior, vol. 37, no 1, , p. 112–118 (PMID 18074216, DOI 10.1007/s10508-007-9272-2, S2CID 41921265).
- ↑ « Chapter V (F) of ICD-10: mental, behavioural and developmental disorders--introduction and overview », Pharmacopsychiatry, vol. 23, no suppl 4, , p. 137–141 (PMID 2197637, DOI 10.1055/s-2007-1014552, S2CID 34081785).
- ↑ « Abnormalities of adult personality and behaviour (section F 6)--results of the ICD-10 field trial », Pharmacopsychiatry, vol. 23, no Suppl 4, , p. 170–172 (PMID 2197643, DOI 10.1055/s-2007-1014559, S2CID 24696932).
- ↑ (de) « [ICD-10 in psychiatric diagnosis. The concept and initial practical experiences] », Versicherungsmedizin, vol. 44, no 4, , p. 114–119 (PMID 1509643).
- ↑ « Psychosexual development of women with congenital adrenal hyperplasia », Hormones and Behavior, vol. 30, no 4, , p. 300–318 (PMID 9047259, DOI 10.1006/hbeh.1996.0038, S2CID 20206538).
- ↑ « Androgen and psychosexual development: core gender identity, sexual orientation and recalled childhood gender role behavior in women and men with congenital adrenal hyperplasia (CAH) », Journal of Sex Research, vol. 41, no 1, , p. 75–81 (PMID 15216426, DOI 10.1080/00224490409552215, S2CID 33519930).
- 1 2 « 2D:4D finger-length ratios in children and adults with gender identity disorder », Hormones and Behavior, vol. 54, no 3, , p. 450–454 (PMID 18585715, DOI 10.1016/j.yhbeh.2008.05.002, S2CID 6324765).
- ↑ « Gender identity outcome in female-raised 46,XY persons with penile agenesis, cloacal exstrophy of the bladder, or penile ablation », Archives of Sexual Behavior, vol. 34, no 4, , p. 423–438 (PMID 16010465, DOI 10.1007/s10508-005-4342-9, S2CID 34971769).
- 1 2 « The intersection of neurotoxicology and endocrine disruption », Neurotoxicology, vol. 33, no 6, , p. 1410–1419 (PMID 22659293, PMCID 3458140, DOI 10.1016/j.neuro.2012.05.014, Bibcode 2012NeuTx..33.1410W).
- ↑ « Prenatal programming of sexual partner preference: the ram model », Journal of Neuroendocrinology, vol. 21, no 4, , p. 359–364 (PMID 19207819, PMCID 2668810, DOI 10.1111/j.1365-2826.2009.01828.x).
- Portail de la sexualité et de la sexologie